Or you want a quick look: Lý thuyết và phương pháp giải bài tập amin oaxit học sinh cần nắm vững
Traloitructuyen.com cũng giúp giải đáp những vấn đề sau đây:
- Bài tập amino axit tác dụng với HCl NaOH
- Bài tập amino axit nâng cao
- Chuyên de bài tập về Amino axit
- Bài tập amino axit trong các de thi đại học
- Các dạng bài tập amino axit có lời giải violet
- Công thức giải nhanh amino axit
- Bài tập đốt cháy amino axit
- Phương pháp giải bài toán amin

Phương pháp giải bài tập đốt cháy amino axit
Lý thuyết và phương pháp giải bài tập amin oaxit học sinh cần nắm vững
I. Amino axit là gì???
Amino axit là hợp chất hữu cơ tạp chức, phân tử chứa đồng thời nhóm amino ( NH2 ) và nhóm cacboxyl ( COOH).
II. Tính chất hóa học của amino axit
+ Tính chất lưỡng tính: Các amin đều phản ứng với axit vô cơ mạnh và bazơ mạnh sinh ra muối tương ứng
+ Tính lưỡng tính axit - bazơ: tùy vào số gốc NH2 và COOH trong phân tử amino axit mà khiến cho quỳ chuyển sang màu hồng ( nhiều gốc COOH hơn) hay chuyển sang màu xanh ( nhiều gốc NH2 hơn)
+ Phản ứng este hóa: Tương tự như axit cacboxylic, amino axit cũng có phản ứng với ancol (xt: H+) tạo este
+ Phản ứng trùng ngưng của ε và ω-amino axit tạo polime thuộc loại poliamit
nH2N−[CH2]5−COOH→−(NH−[CH2]5−CO)−n+nH2O
Axit - aminocaproic policaproamit
III. Tính chất vật lý của amino axit
Thường là chất rắn kết tinh, tương đối dễ tan trong nước và có nhiệt độ nóng chảy cao
IV. Phương trình đốt cháy amino axit tổng quát
CxHyOzNt+2x+y2−z2O2→toxCO2+y2H2O+t2N2
Bảo toàn nguyên tố: C=nCO2naminoaxit; H=2nH2Onaminoaxit
Bảo toàn khối lượng: maa=mC+mH+mO/aa+mN
Bảo toán nguyên tố oxi :nO/aa+2.nCO2=2.nCO2+nH2O
IV. Các amino axit cần nhớ
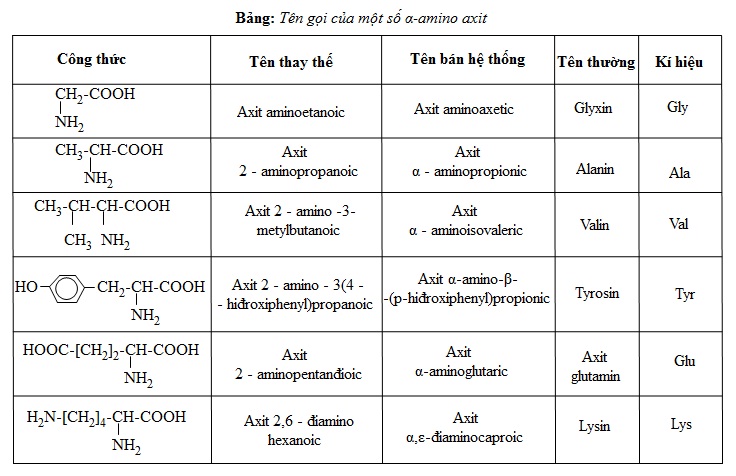
V. Phương pháp giải bài tập amino axit
Phương pháp giải bài tập đốt cháy amino axit tổng quát:
+ Đốt cháy amino axit no, mạch hở, có 1 nhóm amino NH2 và 1 nhóm cacboxyl COOH
CnH2n+1O2N+3n−1,52O2→tonCO2+2n+12H2O+12N2
-> nH2O−nCO2=nN2=12naa
+ Nếu nH2O−nCO2=naminoaxit→ amino axit chứa 1 nhóm COOH và 2 nhóm NH2 hoặc amino axit chứa 2 nhóm COOH và 4 nhóm NH2
+ Nếu nH2O=nCO2 thì amino axit có chứa 2 nhóm COOH và 2 nhóm NH2
+ Khi đốt cháy 1 amino axit ngoài không khi thì:
nN2 sau phản ứng=nN2 sinh ra từ phản ứng đốt cháy amino axit+nN2 có sẵn trong không khí
+ Đốt cháy hỗn hợp amino axit với anken ( hoặc este/axit/ancol có CT dạng CnH2nOx thì luôn có: nH2O−nCO2=nN2=12naa
VI. Bài tập amino axit
Câu 1: Amino axit có khả năng tham gia phản ứng este hóa vì :
A. Amino axit là chất lưỡng tính
B. Amino axit chức nhóm chức – COOH
C. Amino axit chức nhóm chức – NH2
D. Tất cả đều sai
Lời giải chi tiết: Amino axit chứa nhóm -COOH trong phân tử
=> Mang đầy đủ tính chất của axit cacbonxylic, do đó amino axit có phản ứng este hóa
=> Đáp án B
Câu 2: Chất X có công thức phân tử C3H7O2N và làm mất màu dung dịch brom. Tên gọi của X là
A. axit β-aminopropionic B. mety aminoaxetat
C. axit α- aminopropionic D. amoni acrylat
Lời giải chi tiết: X làm mất màu Br2 => X chứa nối đôi C=C
=> X là CH2=CHCOONH4 (Amoni acrylat)
CH2=CHCOONH4+Br2→CH2BrCHBrCOONH4
=> Đáp án D
Câu 3. Hỗn hợp X gồm alanin và axit glutamic. Cho m gam X tác dụng hoàn toàn với dung dịch NaOH (dư), thu được dung dịch Y chứa (m+30,8) gam muối. Mặt khác, nếu cho m gam X tác dụng hoàn toàn với dung dịch HCl, thu được dung dịch Z chứa (m+36,5) gam muối. Giá trị của m là
A. 112,2. B. 165,6. C. 123,8. D. 171,0
Câu 4. Đốt cháy hoàn toàn 45,1 gam hỗn hợp X gồm CH3CH(NH2)COOH và CH3COONH3CH3 thu được CO2, H2O và N2 có tổng khối lượng là 109,9 gam. Phần trăm khối lượng mỗi chất trong hỗn hợp X lần lượt là :
A.39,47% và 60,53% B. 35,52% và 64,48%.
C. 59,20% và 40,80% D. 49,33% và 50,67%
Câu 5. X là một amino axit tự nhiên, 0,01 mol X tác dụng vừa đủ với 0,01 mol HCl tạo muối Y. Lượng Y sinh ra tác dụng vừa đủ với 0,02 mol NaOH tạo 1,11 gam muối hữu cơ Z. X là:
A. axit amino axetic
B. axit β -aminopropionic
C. axit α- aminopropionic
D. axit α- aminoglutaric
Phương trình đốt cháy amino axit tổng quát
CxHyOzNt + 2x+y/2−z2O2 →to xCO2 + y2H2O + t2N2
Bảo toàn nguyên tố : C = nCO2naminoaxit; H = 2nH2Onaminoaxit
Bảo toàn khối lượng: maa = mC + mH + mO/aa + mN
Bảo toàn nguyên tố oxi: nO/aa+ 2.nO2= 2.nCO2+ nH2O
+) Đốt cháy amino axit no, mạch hở, có 1 nhóm amino NH2 và 1 nhóm cacboxyl COOH
CnH2n+1O2N + 3n−1,52O2 →to nCO2 + 2n+12H2O + 12N2
→nH2O−nCO2=nN2=12naa
+ Nếu nH2O – nCO2 = namino axit → amino axit chứa 1 nhóm COOH và 2 nhóm NH2 hoặc amino axit chứa 2 nhóm COOH và 4 nhóm NH2
+ Nếu nH2O = nCO2 thì amino axit có chứa 2 nhóm COOH và 2 nhóm NH2
+ Khi đốt cháy 1 amino axit ngoài không khí thì:
nN2 sau phản ứng = nN2 sinh ra từ phản ứng đốt cháy amino axit + nN2 có sẵn trong không khí
+ Đốt cháy hỗn hợp amino axit với anken (hoặc este/axit/ancol có CT dạng CnH2nOx ) thì luôn có :
Phương pháp giải một số dạng bài tập về amino axit
Dạng 1: Lý thuyết về amino axit
* Một số ví dụ điển hình
Ví dụ 1: Amino axit là hợp chất hữu cơ trong phân tử
A. chứa nhóm cacboxyl và nhóm amino.
B. chỉ chứa nhóm amino.
C. chỉ chứa nhóm cacboxyl.
D. chỉ chứa nitơ hoặc cacbon.
Hướng dẫn giải chi tiết:
Amino axit là hợp chất hữu cơ trong phân tử chứa nhóm cacboxyl và nhóm amino.
Đáp án A.
Ví dụ 2: : Ở điều kiện thường, các amino axit
A. đều là chất khí.
B. đều là chất lỏng.
C. đều là chất rắn.
D. có thể là rắn, lỏng hoặc khí.
Hướng dẫn giải chi tiết:
Amino axit là hợp chất tồn tại ở dạng lưỡng cực : NH3+-R-COO-
=> Ở điều kiện thường, các amino axit đều là chất rắn.
Đáp án C.
Ví dụ 3: pH của dung dịch cùng nồng độ mol của 3 chất H2NCH2COOH, CH3CH2COOH và CH3(CH2)3NH2 tăng theo trật tự nào sau đây ?
A. CH3(CH2)3NH2 < H2NCH2COOH < CH3CH2COOH.
B. CH3CH2COOH < H2NCH2COOH < CH3(CH2)3NH2.
C. H2NCH2COOH < CH3CH2COOH < CH3(CH2)3NH2.
D. H2NCH2COOH < CH3(CH2)3NH2 < CH3CH2COOH.
Hướng dẫn giải chi tiết:
CH3CH2COOH có môi trường axit
NH2CH2COOH có môi trường trung tính
CH3(CH2)3NH2 có môi trường bazo
=> Vậy pH của 3 chất trên được sắp sếp như sau:
CH3CH2COOH < H2NCH2COOH < CH3(CH2)3NH2.
Đáp án B.
Ví dụ 4: : Cho các dãy chuyển hóa : Glyxin →+NaOHX1 →+HCldo¨ X2. Vậy X2 là :
A. H2NCH2COOH.
B. H2NCH2COONa.
C. ClH3NCH2COOH.
D. ClH3NCH2COONa
Hướng dẫn giải chi tiết:
Ta có phương trình phản ứng:
H2NCH2COOH + NaOH → H2NCH2COONa + H2O
H2NCH2COONa + 2HCl → ClH3NCH2COOH + NaCl
Đáp án C
Dạng 2: Bài toán về tính lưỡng tính của amino axit
* Một số lưu ý cần nhớ:
- Amino axit có chứa cả -COOH mang tính axit và –NH2 mang tính bazo nên amino axit có tính lưỡng tính
* Nếu amino axit tác dụng với axit
m Muối = m Amino axit + m Axit
* Nếu amino axit tác dụng với dung dịch kiềm:
m Muối = m Amino axit + m Dung dịch kiềm – m H2O
* Một số ví dụ điển hình:
Ví dụ 1: Cho hỗn hợp 2 aminoaxit no chứa 1 chức axit và 1 chức amino tác dụng với 110 ml dung dịch HCl 2M được dung dịch X. Để tác dụng hết với các chất trong X, cần dùng 140 ml dung dịch KOH 3M. Tổng số mol 2 aminoaxit là :
A. 0,1.
B. 0,2.
C. 0,3.
D. 0.4.
Hướng dẫn giải chi tiết:
2 amin trên có dạng NH2-R-COOH
Ta có sơ đồ quá trình phản ứng như sau:
n HCl = 0,1 * 2 = 0,22 mol
n KOH = 0,14 * 3 = 0,42 mol
Áp dụng định luật bảo toàn nguyên tố Clo
=> n HCl = nKCl = 0,22 (mol)
Áp dụng định luật bảo toàn nguyên tố K
=> n KOH = n KCl + n NH2-R-COOK
=> n NH2-R-COOK = 0,42 – 0,22 = 0,2 (mol)
=> n Amino axit = n NH2-R-COOK = 0,2 (mol)
Đáp án B.
Ví dụ 2: Hợp chất X là một a-amino axit. Cho 0,01 mol X tác dụng vừa đủ với 80 ml dung dịch HCl 0,125M, sau đó đem cô cạn dung dịch thu được 1,835 gam muối. Phân tử khối của X là :
A. 174.
B. 147.
C. 197.
D. 187.
Hướng dẫn giải chi tiết:
n HCl = 0,08 * 0,125 = 0,01 (mol)
Áp dụng định luật bảo toàn khối lượng ta có:
m X + m HCl = m Muối
=> m X = 1,835 – 0,01 * 36,5 = 1,47 (gam)
Khối lượng mol của X là:
1,47 : 0,01 = 147 (gam/mol)
Đáp án B.
Dạng 3: Phản ứng đốt cháy amino axit
* Một ví dụ điển hình:
Ví dụ 1: Khi đốt cháy hoàn toàn một amino axit X là đồng đẳng của axit aminoaxetic, thu được . Công thức cấu tạo thu gọn có thể có của X là :
A. CH3CH(NH2)COOH, H2NCH2CH2COOH.
B. H2N[CH2]3COOH, CH3CH(NH2)CH2COOH.
C. H2N[CH2]4COOH, H2NCH(NH2)[CH2]2COOH.
D. Kết quả khác.
Hướng dẫn giải chi tiết:
X là đồng đẳng của axit amino axetic
=> X là amino axit no, đơn chức mạch hở
CTPT của X có dạng: CnH2n+1NO2
Ta có phương trình đốt cháy:
CnH2n+1NO2 + O2 → n CO2 + (2n+1)/2 H2O + N2
Vì tỉ lệ về thể tích cũng chính là tỉ lệ về số mol
=> V CO2 / V H2O = n : 2n+12= 6 : 7
=> n = 3
=> CTPT của X là: C3H7NO2
CTCT của X có thể có là: CH3CH(NH2)COOH, H2NCH2CH2COOH.
Đáp án A
Ví dụ 2: : Đốt cháy 8,7 gam amino axit X thì thu được 0,3 mol CO2 ; 0,25 mol H2O và 0,05 mol N2 (đktc). CTPT của X là :
A. C3H7O2N.
B. C3H5O2N.
C. C3H7O2N2
D. C3H9O2N2.
Hướng dẫn giải chi tiết:
Áp dụng định luật bảo toàn nguyên tố ta có:
n C = n CO2 = 0,3 mol
n H = 2 n H2O = 0,25 .2 = 0,5 mol
n N = 2 n N2 = 0,05 .2 = 0,1 mol
m O = m X – m C – m H – m O
= 8,7 – 0,3 .12 – 0,5 . 1 – 0,1 . 14 = 3,2 gam
=> n O = 3,2 : 16 = 0,2 mol
Ta có: n C : n H : n N : n O
= 0,3 : 0,5 : 0,1 : 0,2 = 3 : 5 : 1 : 2
=> CTPT của X là : C3H5NO2
Đáp án B
Bài viết hướng dẫn các em cách giải một số bài tập đốt cháy amino axit.
BÀI TẬP ĐỐT CHÁY AMINO AXIT
CTTQ + Amino axit no, có 1 nhóm amino NH2
1 nhóm cacboxyl COOH
NH2- CmH2m – COOH hoặc CnH2n+1O2N
+ Amino axit: CxHyOzNt
CxHyOzNt + O2 → CO2 + H2O + N2
maa = mC + mH + mO/aa + mN
BTNT oxi: nO/aa + 2. nO2 = 2. nCO2 + nH2O
Chú ý
+ Nếu nH2O – nCO2= namino axit => amino axit chứa 1 nhóm COOH và 2 nhóm NH2 hoặc amino axit chứa 2 nhóm COOH và
4 nhóm NH2
+ Nếu nH2O = nCO2thì amino axit có chứa 2 nhóm COOH và 2 nhóm NH2
Ví dụ 1. Đốt cháy hoàn toàn 8,7 g amino axit A (chứa 1 nhóm -COOH) thì thu được 0,3 mol CO2; 0,25mol H2O và 11,2 lít N2 (đktc). Tìm CTCT A
Lời giải
CTPT: CxHyOzNt , nN2 = 0,05 mol
[external_link offset=1]
nO/aa = (8,7 – 0,3 .12 – 0,+84888672676 – 0,+84888672676) : 16 = 0,2 mol
naa = nO / 2 = 0,1 mol
x = 0,3 / 0,1 = 3
y = 2nH2O / naa = 5
z = 2nN2 / naa = 1
=> CTPT C3H5O2N
CH3- CH2 (NH2)-COOH
H2N- CH2 – CH2 - COOH
Ví dụ 2: Hỗn hợp X gồm 1 mol aminoaxit no, mạch hở và 1 mol amin no, mạch hở. X có khả năng phản ứng tối đa với 2 mol HCl hoặc 2 mol NaOH. Đốt cháy hoàn toàn X thu được 6 mol CO2, x mol H2O và y mol N2. Các giá trị x, y tương ứng là
- A. 7 và 1,0. B. 8 và 1,5. C. 8 và 1,0. D. 7 và 1,5.
Lời giải
Aminoaxit là CmH2m -1O4N, amin là CnH2n+3N
Phản ứng cháy: CmH2m -1O4N m CO2 + H2O +N2
CnH2n+3N nCO2 + H2O + N2
Số mol CO2 là : n+m =6 nH2O = n + m+ 1 = 7. Số mol N2 = 1. Chọn đáp án A
Ví dụ 3. Đốt cháy hoàn toàn 0,5 mol hỗn hợp X gồm 2 chất H2NR(COOH)x và CnH2n+1COOH, thu được 52,8 gam CO2 và 24,3 gam H2O. Mặt khác, 0,1 mol X phản ứng vừa đủ với dung dịch chứa a mol HCl. Giá trị của a là
Lời giải
Ta có nCO2 = 1,2 mol; nH2O = 1,35 mol.
=> amino axit là no, đơn chức (vì axit có nCO2 = nH2O)
Đặt công thức chung là amino axit là CmH2m+1O2N, viết phương trình đốt cháy ta có:
CmH2m+1O2N + xO2 → mCO2 + (2m+1)/2 H2O
a mol ma (2m+1)a/2
=> 2(nH2O – nCO2) = (2m+1)a – 2ma = a
=> Số mol amino axit là: n = 2 (1,35 – 1,2) = 0,3 mol => chiếm 3/5
[external_link offset=2]
=> Với 0,1 mol X phản ứng thì có 0,06 mol amino axit
=> nHCl = 0,06 mol
BÀI TẬP ÁP DỤNG
Câu 1. Đốt cháy hoàn toàn một lượng chất hữu cơ X thu được 3,36 lít khí CO2 và 0,56 lít khí N2 (các khí đo ở đktc) và 3,15 gam H2O. Khi X tác dụng với dung dịch NaOH thu được sản phẩm trong đó có muối H2N–CH2–COONa. Công thức cấu tạo thu gọn của X là
A. H2N–CH2COO–C3H7. B. H2N–CH2COO–CH3.
C. H2N–CH2CH2COOH. D. H2N–CH2COO–C2H5.
Câu 2. Đipeptit mạch hở X và tripeptit mạch hở Y đều được tạo nên từ một aminoaxit (no, mạch hở, trong phân tử chứa một nhóm –NH2 và một nhóm –COOH). Đốt cháy hoàn toàn 0,1 mol Y, thu được tổng khối lượng CO2 và H2O bằng 54,9 gam. Đốt cháy hoàn toàn 0,2 mol X, sản phẩm thu được cho lội từ từ qua nước vôi trong dư, tạo ra m gam kết tủa. Giá trị của m là
A. 45 g. B. 60 g. C. 120 g. D. 30 g.
Câu 3. Hỗn hợp X gồm 2 amino axit no (chỉ có nhóm chức –COOH và –NH2 trong phân tử), trong đó tỉ lệ mO : mN = 80 : 21. Để tác dụng vừa đủ với 3,83 gam hỗn hợp X cần 30 ml dung dịch HCl 1M. Mặt khác, đốt cháy hoàn toàn 3,83 gam hỗn hợp X cần 3,192 lít O2 (đktc). Dẫn toàn bộ sản phẩm cháy (CO2, H2O và N2) vào nước vôi trong dư thì khối lượng kết tủa thu được là
A. 20 gam. B. 13 gam. C. 10 gam. D. 15 gam.
Câu 4. Peptit X bị thủy phân theo phương trình phản ứng X + 2H2O → 2Y + Z (trong đó Y và Z là các amino axit). Thủy phân hoàn toàn 4,06 gam X thu được m gam Z. Đốt cháy hoàn toàn m gam Z cần vừa đủ 1,68 lít khí O2 (đktc), thu được 2,64 gam CO2; 1,26 gam H2O và 224 ml khí N2 (đktc). Biết Z có công thức phân tử trùng với công thức đơn giản nhất. Tên gọi của Y là
A. glyxin B. lysin C. axit glutamic D. alanin
Câu 5. Đốt cháy hoàn toàn m gam một amin X bằng lượng không khí vừa đủ thu được 17,6 gam CO2, 1,26 gam H2O và V lít N2 (đktc). Giả sử không khí chỉ gồm N2 và O2 trong đó O2 chiếm 20% thể tích. Công thức phân tử của X và giá trị của V lít lần lượt là
- X: C2H5NH2 và V = 6,72 lít C. X: C3H7NH2 và V = 6,72 lít
- X: C3H7NH2 và V = 6,94 lít D. X: C2H5NH2 và V = 4,704 lít
ĐÁP ÁN
1. B 2. C 3. B 4. A 5. D
Traloitructuyen.com cũng giúp giải đáp những vấn đề sau đây:
- Bài tập amino axit tác dụng với HCl NaOH
- Bài tập amino axit nâng cao
- Chuyên de bài tập về Amino axit
- Bài tập amino axit trong các de thi đại học
- Các dạng bài tập amino axit có lời giải violet
- Công thức giải nhanh amino axit
- Bài tập đốt cháy amino axit
- Phương pháp giải bài toán amin

